دانلود کتاب نگرشی بر طیف سنجی پاویا ترجمه فارسی توسط فریما قدمی ترجمه شده است.این کتاب ثبت اثر شده و دارای کد شامد می باشد.هر گونه کپی برداری از تمام و یا قسمتی از محصول و انتشار غیر قانونی آن توسط افراد سودجو، بدون تذکر قبلی، پیگرد قانونی در پی خواهد داشت.
دانلود کتاب نگرشی بر طیف سنجی پاویا لپیمن و کریز ویویان ترجمه فارسی
کاربران گرامی،محصول مورد نظر شامل کتاب نگرشی بر طیف سنجی پاویا لپیمن و کریز ویویان ترجمه فارسی با کیفیت بسیار بالا تایپ شده به صورت رنگی و با قابلیت سرچ می باشد که با فرمت پی دی اف به زبان فارسی در حجم 883 صفحه با کیفیت عالی در اختیار شما عزیزان قرار گرفته است.در صورت تمایل می توانید این محصول را از سایت خریداری و دانلود نمائید.
طیفسنجی یک روش تجزیه و تحلیل است که در آن نور یا امواج الکترومغناطیسی به یک نمونه ارسال میشود و سپس واکنش نمونه بازتابی از نور را دریافت میکند. این روش اطلاعات مفیدی را در مورد خصوصیات فیزیکی و شیمیایی نمونه فراهم میکند. با استفاده از طیفسنجی، میتوان مواردی مانند ترکیبات مولکولی، ساختار دقیق، و ویژگیهای الکترونیکی مواد را تعیین کرد. این روش در زمینههای مختلفی از جمله شیمی، فیزیک، زیستشناسی، و علوم مواد به کار میرود.
اما فرد اتم نیتروژن باشد منجر میشود که مقدار U عددی کسری شود که بسیار نادر است.
هر ترکیبی با مقدار U کمتر از صفر (عدد منفی) یک ترکیب غیرممکن است. چنین مقداری اغلب نشانگر این است که یک اتم اکسیژن یا نیتروژن نیز باید در فرمول مولکولی وجود داشته باشد. وقتی فرمولها را با استفاده از این روش محاسبه میکنیم، اگر هیدروژن کافی نباشد، میتوانیم 1 کربن کم کرده و 12 هیدروژن اضافه کنیم (و تصحیح مناسب را برای U انجام دهیم). این روش تنها در صورتی کار میکند که مقدار U را مثبت به دست آورده باشیم. همچنین، میتوانیم با افزودن 1 کربن و کم کردن 12 هیدروژن (و تصحیح U) مولکول بالقوه دیگری نیز بدست آوریم.
دانلود کتاب نگرشی بر طیف سنجی پاویا فارسی
1.6 قانون نیتروژن
قانون دیگری که میتوان در تعیین فرمول مولکولی از آن استفاده کرد، قانون نیتروژن است. این قانون بیان میکند که وقتی تعداد اتمهای نیتروژن موجود در مولکول فرد باشد، جرم مولکولی نیز یک عدد فرد خواهد بود. وقتی تعداد اتم های نیتروژن موجود در مولکول زوج (یا صفر) باشد، جرم مولکولی یک عدد زوج خواهد بود. قانون نیتروژن در فصل 3، بخش 3.6 بیشتر توضیح داده شده است.

چالش ها و مسائل
1. محققان از روش احتراق برای تجزیه و تحلیل ترکیبی استفاده کردند که به عنوان یک ماده افزودنی ضد ضربه در بنزین استفاده میشود. یک نمونه 9.394 میلی گرمی از این ترکیب، 31.154 میلی گرم دی اکسید کربن و 7.977 میلی گرم آب در احتراق به دست میدهد.
الف) درصد ترکیب ماده را محاسبه کنید. (ب) فرمول تجربی آن را تعیین کنید.
2. احتراق یک نمونه 8.23 میلی گرمی از ماده ناشناخته، 9.62 میلی گرم CO2 و 3.94 میلی گرم H2O به دست آورد. نمونه دیگری با وزن 5.32 میلی گرم، 13.49 میلی گرم AgCl را هنگام تجزیه هالوژن، تولید کرد. درصد ترکیب و فرمول تجربی این ترکیب آلی را تعیین کنید.
3. درصد ترکیب اسید آمینه C32.00٪، H6.71٪، و N18.66٪. فرمول تجربی این ماده را محاسبه کنید.
4. هنگامی که ترکیبی از 02/5 میلیگرم ماده ناشناخته و 37/50 میلیگرم کافور تهیه شد، نقطه ذوب بخشی از این مخلوط تعیین شد. نقطه ذوب مشاهده شده برای مخلوط 156 کربن بود. جرم مولکولی این ماده چقدر است؟
5. یک اسید ناشناخته با 23.1 میلی لیتر از 0.1 N هیدروکسید سدیم تیتر شد. وزن اسید 120.8 میلی گرم بود. وزن معادل اسید چقدر است؟
6. تعیین شاخص کمبود هیدروژن را برای هر یک از ترکیبات زیر بدست آورید: (الف) C8H7NO (د) C5H3ClN4
(ب) C3H7NO3 (ه) C21H22N2O2
(C) C4H4BrNO2
7. یک ماده دارای فرمول مولکولی C4H9N است. آیا این احتمال وجود دارد که این ماده دارای پیوند سه گانه باشد؟ استدلال خود را توضیح دهید.
دانلود رایگان کتاب طیف سنجی پاویا
8. (الف)
محققی یک جامد ناشناخته استخراج شده از پوست درختان صنوبر را برای تعیین درصد ترکیب آن تجزیه و تحلیل کرد. یک نمونه 11.32 میلی گرمی در دستگاه احتراق سوزانده شد. دی اکسید کربن (24.87 میلی گرم) و آب (5.82 میلی گرم) جمعآوری شد. از نتایج این تجزیه و تحلیل، درصد ترکیب جامد ناشناخته را محاسبه کنید.
(ب) فرمول تجربی جامد مجهول را تعیین کنید.
(ج) از طریق طیف سنجی جرمی، جرم مولکولی 420 گرم در مول تعیین شد. فرمول مولکولی این ماده چیست؟
(د) این ترکیب چند حلقه معطر میتواند داشته باشد؟
9. فرمول مولکولی احتمالی ترکیباتی با جرم مولکولی 136 را محاسبه کنید. از قانون سیزده استفاده کنید ممکن است فرض کنید که تنها اتم های دیگر موجود در هر مولکول کربن و هیدروژن هستند.
الف) ترکیبی با دو اتم اکسیژن
ب) ترکیبی با دو اتم نیتروژن
ج) ترکیبی با اتمهای نیتروژن و بدون هیچ اکسیژنی
د) ترکیبی با پنج اتم کربن و چهار اتم اکسیژن
طیفسنجی در انواع مختلفی وجود دارد از جمله:
طیفسنجی UV-Vis: در این روش، نور مرئی و فرابنفش به نمونه ارسال میشود و جذب نمونه در این محدوده از طیف بررسی میشود. این روش برای تعیین غلظت واکنشگرها و تحقیقات در زمینه رنگها و فرایندهای شیمیایی مورد استفاده قرار میگیرد.
طیفسنجی فروسرخ (IR): در این روش، امواج فروسرخ به نمونه ارسال میشود که توسط گروههای عاملی در مولکولها جذب میشود. این روش برای تعیین ساختار مولکولی و شناسایی گروههای عاملی در مولکولها استفاده میشود.
طیفسنجی رزونانس مغناطیسی هستهای (NMR): این روش بر مبنای تابع فیزیکی اتصال مغناطیسی هستهای با یک میدان مغناطیسی خارجی است. طیفهای NMR برای تعیین ساختار مولکولی، تعیین ترکیبات شیمیایی، و بررسی پویایی مولکولها مورد استفاده قرار میگیرند.
طیفسنجی ابزاری قدرتمند در دانش علوم طبیعی و مهندسی است که به محققان امکان میدهد تا خصوصیات مختلف مواد را به دقت بررسی کنند و از آنها در تحقیقات خود استفاده کنند.
طیفسنجی رامان: در این روش، نور لیزر به نمونه ارسال میشود و نور پراکنده شده توسط نمونه بررسی میشود. این روش برای تعیین ترکیبات شیمیایی، ساختار مولکولی، و شناسایی فازهای مختلف مواد استفاده میشود.
طیفسنجی فلورسانس: در این روش، نمونه با نوری محرکه تحت تأثیر قرار میگیرد و سپس نور فلورسانس از نمونه جذب شده و انتشار مییابد. این روش برای شناسایی مواد فلورسانت و بررسی تغییرات ساختاری و محیطی مواد استفاده میشود.
طیفسنجی ماهوارهای: در این روش، از دادههای طیفی که از ماهوارهها دریافت میشود برای بررسی جزئیات جوی و زمینشناسی سیارهها استفاده میشود.
طیفسنجی الکترونی: در این روش، جذب و انتشار الکترونها توسط نمونه بررسی میشود که اطلاعاتی در مورد ویژگیهای الکترونیکی مواد فراهم میکند.
10. یک الکالوئید از یک نوشیدنی معمولی خانگی جدا شد. مشخص شد که آلکالوئید ناشناخته دارای جرم مولکولی 194 است. با استفاده از قانون سیزده، فرمول مولکولی و شاخص کمبود هیدروژن را برای این ماده تعیین کنید. آلکالوئیدها مواد آلی طبیعی هستند که حاوی نیتروژن هستند. (نکته: در فرمول مولکولی آنها چهار اتم نیتروژن و دو اتم اکسیژن وجود دارد. کافئین ماده ناشناخته است. ساختار این ماده را در فهرست مرک جستجو و فرمول مولکولی آن را مشخص کنید.)
11. اداره مبارزه با مواد مخدر (DEA) در جریان یک ماموریت، یک ماده توهم زا را کشف و ضبط کرد. هنگامی که شیمیدانان DEA ماده توهم زای ناشناخته را مورد تجزیه و تحلیل شیمیایی قرار دادند، دریافتند که این ماده دارای جرم مولکولی 314 است. تجزیه و تحلیل عنصری فقط وجود کربن و هیدروژن را نشان داد. با استفاده از قانون سیزده، فرمول مولکولی و شاخص کمبود هیدروژن را برای این ماده تعیین کنید. (نکته: فرمول مولکولی ماده مجهول حاوی دو اتم اکسیژن نیز هست. ماده ناشناخته ، تتراهیدروکانابینول، ماده فعال ماری جوانا است. ساختار تتراهیدروکانابینول را در فهرست مرک جستجو و فرمول مولکولی آن را مشخص کنید.)
دانلود رایگان کتاب نگرشی بر طیف سنجی پاویا
12.یک کربوهیدرات از نمونه شیر گاو جدا شد. این ماده دارای جرم مولکولی 342 است. کربوهیدرات ناشناخته را می توان هیدرولیز کرد تا دو ترکیب ایزومر تشکیل دهد، هر کدام از این ایزومرها دارای جرم مولکولی 180 هستند. دانلود کتاب شیمی فیزیک اتکینز جلد 1 و 2 فارسی با استفاده از قانون سیزده، فرمول مولکولی و شاخص کمبود هیدروژن را برای ماده ناشناخته و محصولات حاصل از هیدرولیز آن تعیین کنید. (نکته: با حل فرمول مولکولی محصولات حاصل از هیدرولیز 180 گرم از ماده شروع کنید. این محصولات به ازای هر اتم کربن، یک اتم اکسیژن نیز در فرمول مولکولی دارند. ماده ناشناخته لاکتوز است. ساختار آن را در فهرست مرک جستجو و فرمول مولکولی آن را تأیید کنید.)
پاسخ ها در فصل پاسخ به مسائل منتخب ارائه شده است.
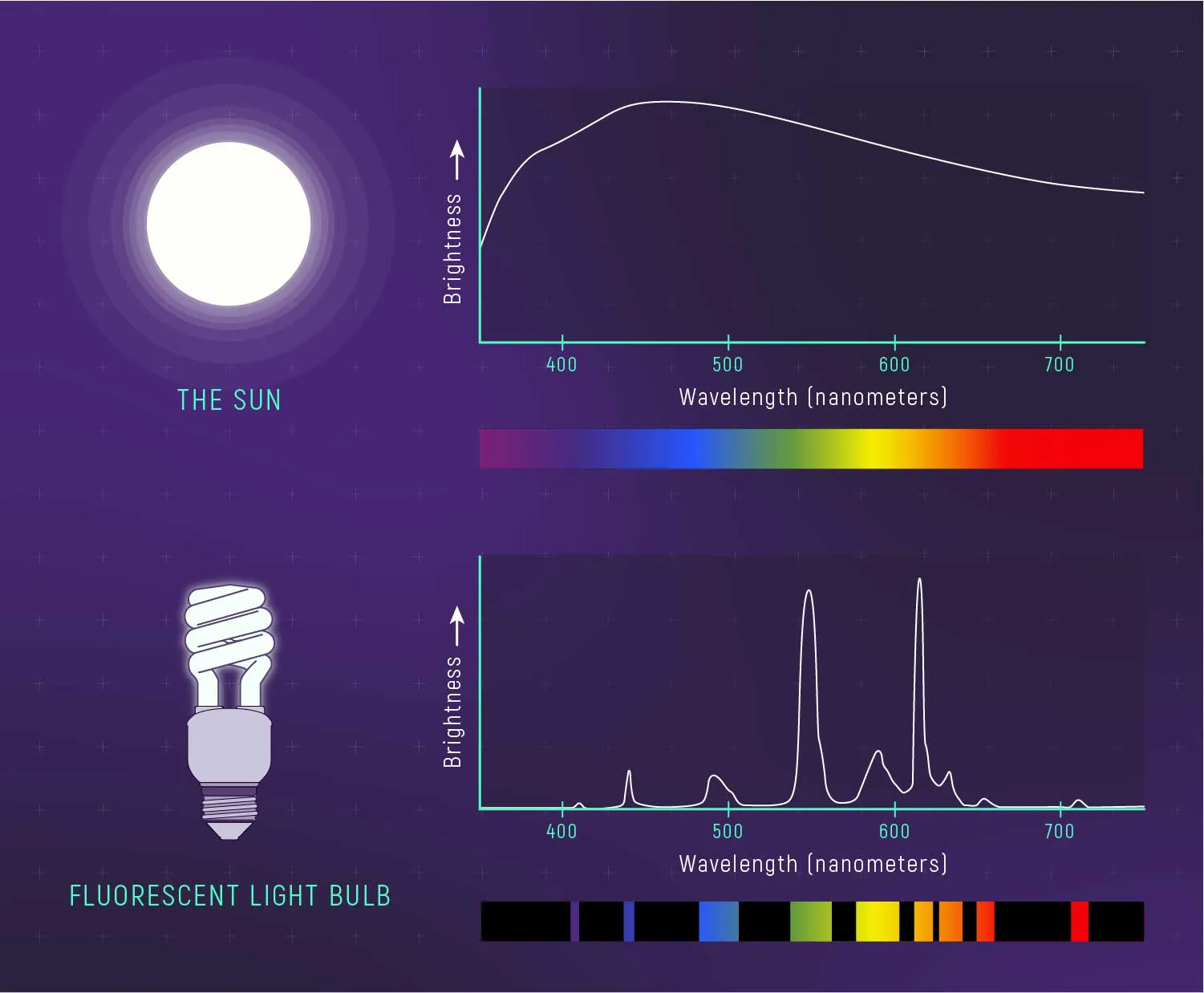
تقریباً هر ترکیبی که دارای پیوند کووالانسی باشد، چه آلی یا معدنی، فرکانس های مختلف تابش الکترومغناطیسی را در ناحیه مادون قرمز طیف الکترومغناطیسی جذب میکند. این ناحیه در طول موجهایی بیشتر از طول موجهای مرتبط با نور مرئی قرار دارد که از حدود 400 تا 800 نانومتر (1 نانومتر = 10 به توان منفی9 متر) متغیر هستند، اما در طول موجهای کوتاهتر از امواج مایکروویو که بیشتر از 1 میلیمتر هستند، قرار دارد. اهداف شیمیایی اصلی این موضوع، در بخش ارتعاشی منطقه مادون قرمز مطرح شده. این شامل تابشی با طول موج (l) بین 2.5 تا 25 میکرومتر (1 میلی متر = 10-6 متر) است. اگرچه واحد صحیح تر برای طول موج ناحیه مادون قرمز طیف، میکرومتر است، اما اغلب واحد میکرون را هنگام مطالعه درمورد طیف مادون قرمز مشاهده خواهید کرد. شکل 2.1 رابطه ناحیه مادون قرمز و سایر مناطق موجود در طیف الکترومغناطیسی نشان میدهد.
شکل 2.1 نشان می دهد که طول موج l با فرکانس n نسبت معکوس دارد و توسط رابطه n = c/l، که در آن c = سرعت نور، کنترل میشود. همچنین توجه کنید که انرژی با فرکانس نسبت مستقیم دارد: E = hn، که در آن h = ثابت پلانک. از معادله اخیر، می توانید ببینید که از نظر کیفی بیشترین تابش انرژی مربوط به ناحیه پرتو ایکس طیف است، جایی که انرژی لازم برای شکستن پیوندها در مولکول ها وجود داشته باشد. در انتهای دیگر طیف الکترومغناطیس، فرکانسهای رادیویی انرژی بسیار پایینی دارند، به اندازهای که فقط باعث انتقال اسپین هستهای یا الکترونیکی در مولکولها شوند – به ترتیب رزونانس مغناطیسی هستهای (NMR) یا رزونانس اسپین الکترون (ESR).
در جدول 2.1 نواحی طیف و انواع انتقال انرژی مشاهده شده در آن، خلاصه شده. تعدادی از این مناطق، از جمله ناحیه مادون قرمز، اطلاعاتی حیاتی در مورد ساختار مولکول های آلی به دست می دهند. رزونانس مغناطیسی هستهای، که در قسمت فرکانس رادیویی طیف رخ می دهد، در فصل های 5 تا 9 مورد بحث قرار گرفته است، به طیف سنجی فرابنفش و مرئی نیز در فصل 10 پرداخته شده است.
طیفسنجی فلورسانس (Fluorescence): در این روش، نمونه با نوری با طول موج معین تحت تابش قرار میگیرد و نوری با طول موج دیگر از آن گسیل میشود. این روش برای تعیین غلظت و تشخیص مواد فلورسانت در نمونهها استفاده میشود، که در زمینههایی از جمله بیوشیمی، داروسازی و علوم مواد مورد استفاده قرار میگیرد.
طیفسنجی نوسان (Raman): در این روش، نمونه با لیزر تحت تابش قرار میگیرد و نور پراکنده شده توسط مولکولهای نمونه بررسی میشود. طیفسنجی رامان برای تعیین ساختار مولکولی، شناسایی ترکیبات شیمیایی و بررسی ویژگیهای فیزیکی مواد استفاده میشود.
طیفسنجی جذب اتمی (Atomic Absorption Spectroscopy): در این روش، جذب نور توسط اتمهای یک عنصر خاص در نمونه بررسی میشود. این روش برای تعیین غلظت عناصر فلزی در نمونهها استفاده میشود و در آنالیز مواد معدنی، آب، و مواد غذایی کاربرد دارد.
طیفسنجی جذبی پلاسمایی (Inductively Coupled Plasma Optical Emission Spectroscopy – ICP-OES): در این روش، نمونه با استفاده از پلاسمای جفت شده و نوری به آن ارسال میشود و جذب نور توسط عناصر در نمونه اندازهگیری میشود. این روش برای تعیین غلظت عناصر فلزی در نمونههای مختلف، از جمله آب، خاک، و نمونههای زیستی مورد استفاده قرار میگیرد.
طیفسنجی امپدانس الکتروشیمیایی (Electrochemical Impedance Spectroscopy – EIS): این روش در زمینههای برق شیمیایی و سنتز مواد الکترونیکی کاربرد دارد. با استفاده از EIS، میتوان اطلاعاتی در مورد رفتار الکتروشیمیایی سطح نمونه و فرایندهای الکترودیک آن را بدست آورد.
شیمیدانان برای تابش در ناحیه مادون قرمز ارتعاشی طیف الکترومغناطیسی بیشتر واحدی به نام عدد موج (وی بار) را به کار میبرند، تا طول موج (میکرون یا میکرومتر).
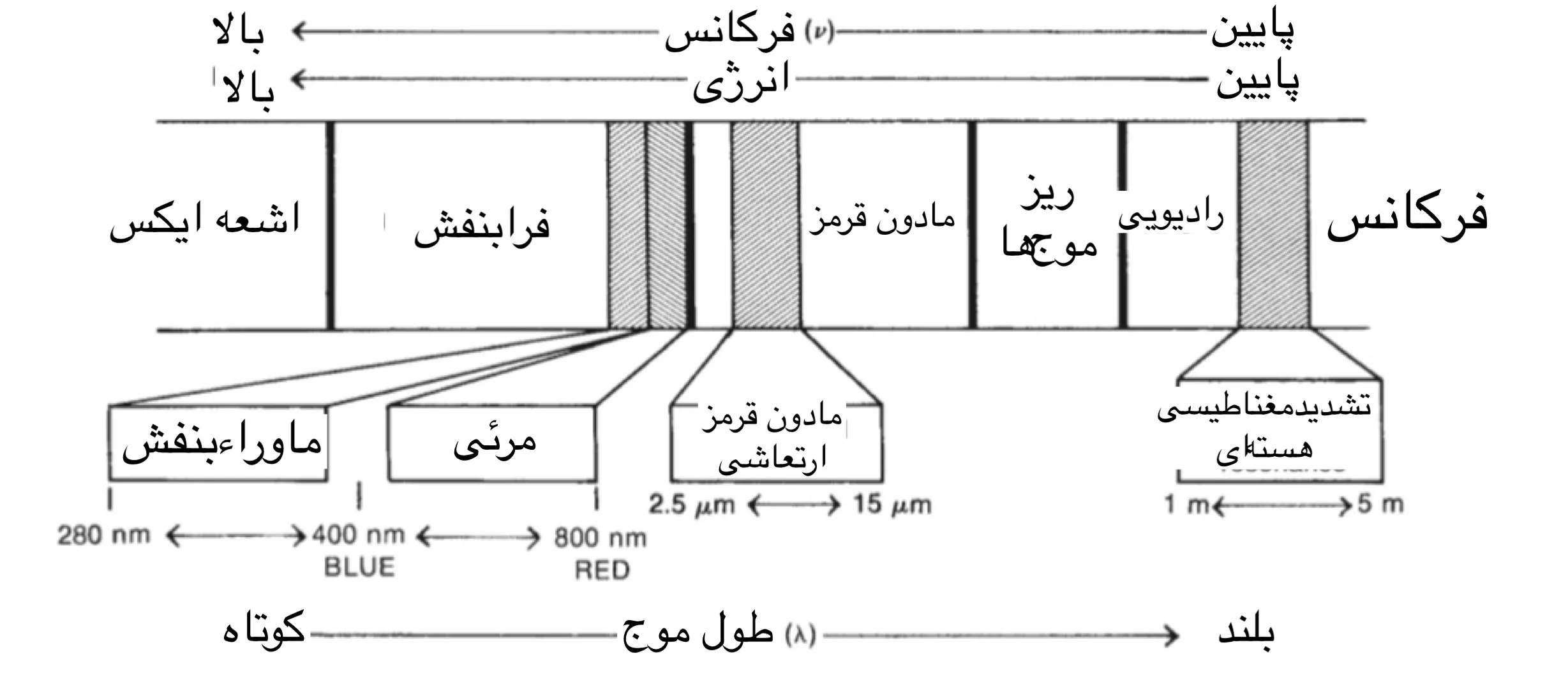
شکل 2 . 1 بخشی از طیف الکترومغناطیسی است که جایگاه مادون قرمز ارتعاشی و سایر انواع تابشها را نشان می دهد. 2.1 فرآیند جذب مادون قرمز

اعداد موج به صورت سانتیمتر متقابل (cm-1) بیان میشوند و به راحتی با تقابل گرفتن از طول موج بیان شده در واحد سانتی متر محاسبه میشوند. یک عدد موج (vبار) با ضرب در سرعت نور (سانتی متر بر ثانیه) به فرکانس v تبدیل میشود.
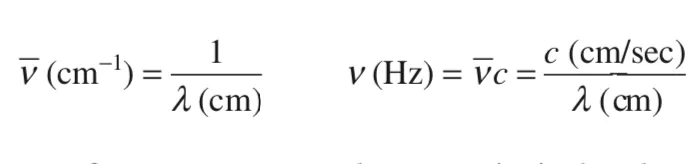
علت اصلی که بخاطر آن، شیمیدانان ترجیح میدهند از عددموج به عنوان واحد استفاده کنند این است که تغییرات آنها نسبت مستقیمی با تغییرات انرژی دارد (عدد موج بالاتر مربوط به انرژی بالاتر است). بنابراین، از نظر عدد موج، مادون قرمز ارتعاشی از حدود 4000 تا 400 سانتیمتر-1 گسترش می یابد. این محدوده مربوط به طول موج 2.5 تا 25 میکرومتر است. ما در این کتاب درسی منحصرا از واحد عدد موج استفاده خواهیم کرد. ممکن است در منابع قدیمی با مقادیر طول موج روبرو شوید. با استفاده از روابط زیر، طول موج (میکرون یا میکرومتر) را به عدد موج (cm-1) تبدیل کنید:
2.1 فرآیند جذب مادون قرمز
مولکول ها با جذب تابش مادون قرمز به موقعیتی با انرژی بالاتر برانگیخته میشوند. جذب تابش مادون قرمز مانند سایر فرآیندهای جذب، یک فرآیند کوانتیزه است. یک مولکول فقط فرکانسهای خاصی (انرژی) از اشعه مادون قرمز را جذب میکند.
دانلود کتاب طیف سنجی پاویا pdf
با جذب تابش مادون قرمز، حدود 8 تا 40 کیلوژول تغییر انرژی داریم. تابش در این محدوده انرژی، مربوط به فرکانسهای ارتعاشی کششی و خمشی پیوندها در اکثر مولکولهایی با پیوند کووالانسی است. در فرآیند جذب، آن دسته از فرکانسهای تابش مادون قرمز که با فرکانسهای ارتعاشی طبیعی مولکول مورد نظر مطابقت دارند، جذب میشوند و انرژی جذبشده منجر به افزایش دامنه حرکات ارتعاشی پیوندهای مولکول میشود.
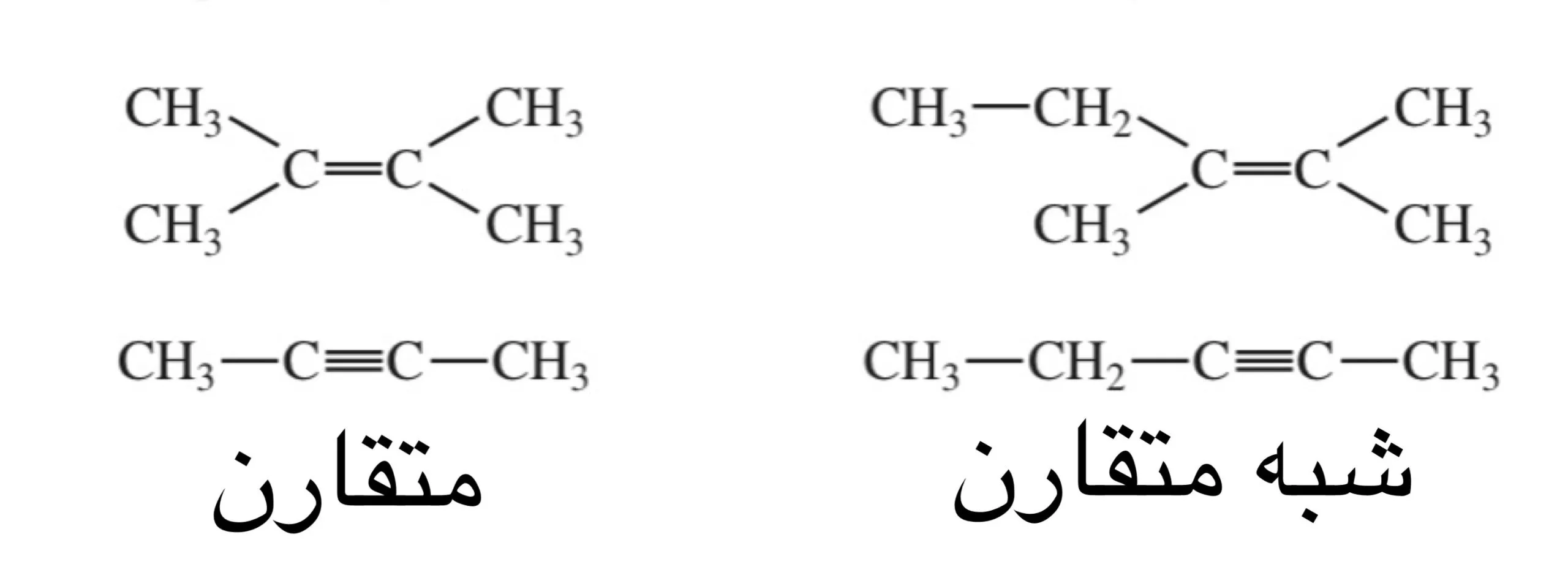
البته توجه داشته باشید که همه پیوندهای موجود در یک مولکول قادر به جذب انرژی مادون قرمز نیستند، حتی اگر فرکانس تابشی مطابق با فرکانس جدایی پیوند داشته باشد. تنها پیوندهای دارای گشتاور دوقطبی که بر حسب زمان تغییر میکنند، قادر به جذب تابش مادون قرمز هستند. پیوندهای متقارن، مانند پیوندهای H2 یا Cl2، تابش مادون قرمز را جذب نمی کنند.
یک پیوند باید یک دوقطبی الکتریکی داشته باشد که با فرکانس مشابه تابش ورودی تغییر کند تا بتواند انرژی را جذب کند. سپس دوقطبی الکتریکی در حال تغییر پیوند میتواند با میدان الکترومغناطیسی سینوسی در حال تغییر تابش ورودی هماهنگ شود. بنابراین، یک پیوند متقارن که دارای گروه های یکسان یا تقریباً یکسان در هر انتها باشد، مادون قرمز را جذب نمیکند.
یک شیمیدان آلی باید بداند؛ پیوندهایی که احتمالاً تحت تأثیر این محدودیت قرار می گیرند پیوندهای آلکن های متقارن یا شبه متقارن (پیوند یگانه کربن-کربن) و آلکین ها (پیوند دوگانه کربن-کربن) هستند.
2.2 استفاده از طیف مادون قرمز
از آنجایی که هر نوع پیوندی دارای فرکانس طبیعی ارتعاش متفاوتی است و دو نوع پیوند مشابه در دو ترکیب متفاوت، تاحدی با هم فرق دارند، هیچ دو مولکولی با ساختار متفاوت دقیقاً الگوی جذب طیف فروسرخ مشابهی ندارند. اگرچه برخی از فرکانس های جذب شده در این دو مورد ممکن است یکسان باشند، اما در هیچ موردی از دو مولکول مختلف، طیف مادون قرمز آنها (الگوهای جذب) یکسان نخواهد بود. بنابراین، طیف مادون قرمز را میتوان همانطور که از اثر انگشت برای شناسایی انسان استفاده کرد، به کار برد. با مقایسه طیف مادون قرمز دو ماده که تصور میشود یکسان هستند، می توانید مشخص کنید که آیا آنها در واقع یکسان هستند یا خیر. اگر طیف مادون قرمز آنها نقطه به نقطه (جذب برای جذب) منطبق باشد، در بیشتر موارد این دو ماده یکسان خواهند بود.
طیفسنجی یکی از مهمترین و کاربردیترین تکنیکهای آنالیز و مطالعه مواد است که در انواع مختلف علوم از شیمی و فیزیک تا زیستشناسی و علوم مهندسی استفاده میشود. این تکنیک بر پایه بررسی و تجزیه و تحلیل انتشار یا جذب نور یا امواج الکترومغناطیسی توسط مواد بنیادی شده است. هدف اصلی از انجام طیفسنجی، شناسایی و تحلیل ترکیبات شیمیایی و ویژگیهای فیزیکی مواد مختلف است. از این رو، این تکنیک از اهمیت بسزایی در تحقیقات پایه و کاربردهای صنعتی برخوردار است.
دانلود کتاب طیف سنجی پاویا
دومین و مهمترین کاربرد طیف مادون قرمز، تعیین اطلاعات ساختاری در مورد یک مولکول است. جذب هر نوع پیوند (NIH، CIH، OIH، CIX، CJ O، CIO، CIC، CJ C، CK C، CK N، و غیره) به طور منظم فقط در بخش های کوچک و خاصی از مادون قرمز ارتعاشی یافت میشود. برای منطقه هر نوع پیوندی میتوان محدوده کوچکی از جذب را تعریف کرد. جذب در خارج از این محدوده، معمولاً به دلیل نوع دیگری از پیوند است.
به عنوان مثال، هر گونه جذب در محدوده 150 ± 3000 سانتی متر-1 تقریباً همیشه به دلیل وجود پیوند CH در مولکول است. یک جذب در محدوده 100 ± 1715 سانتی متر-1 معمولاً به دلیل وجود پیوند C=O (گروه کربونیل) در مولکول است. همان نوع محدوده برای هر نوع پیوندی اعمال می شود. شکل 2.2 به طور شماتیک نشان میدهد که چگونه این پیوندها بر روی مادون قرمز ارتعاشی پخش می شوند. سعی کنید برای راحتی کار خود، این طرح کلی را در ذهن داشته باشید.
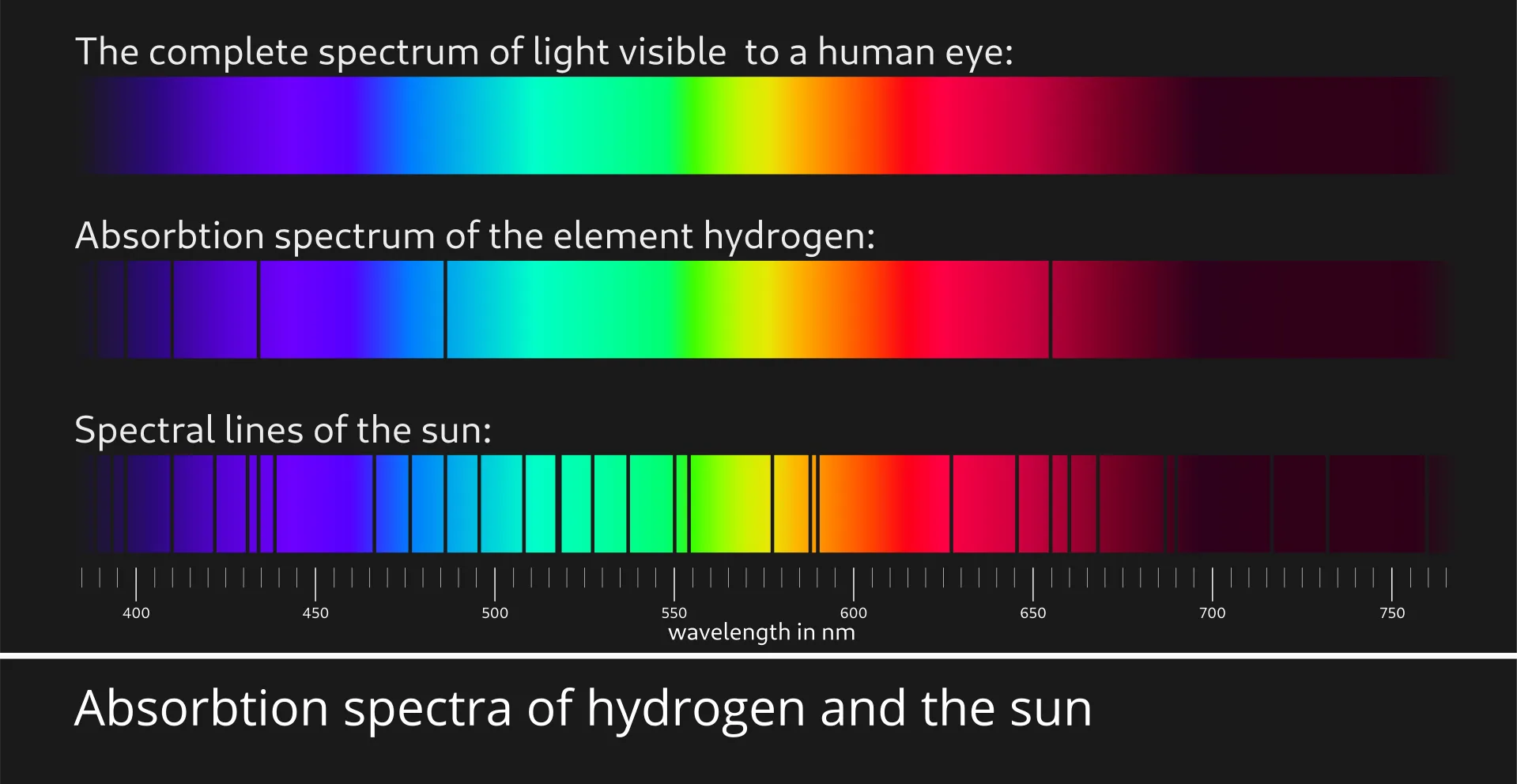
شکل 2 . 2 مناطق تقریبی که در آن انواع رایج پیوندها جذب میشوند (ارتعاشات کششی؛ خم شدن، پیچش و سایر انواع ارتعاشات پیوند برای ملموس شدن موضوع، حذف شدهاند).
3 حالت های کشش و خم شدن
2.3 حالت های کشش و خم شدن
سادهترین نوع یا حالتهای حرکت ارتعاشی در یک مولکول فعال مادون قرمز – آنهایی که باعث جذب میشوند – حالتهای کشش و خمش هستند.
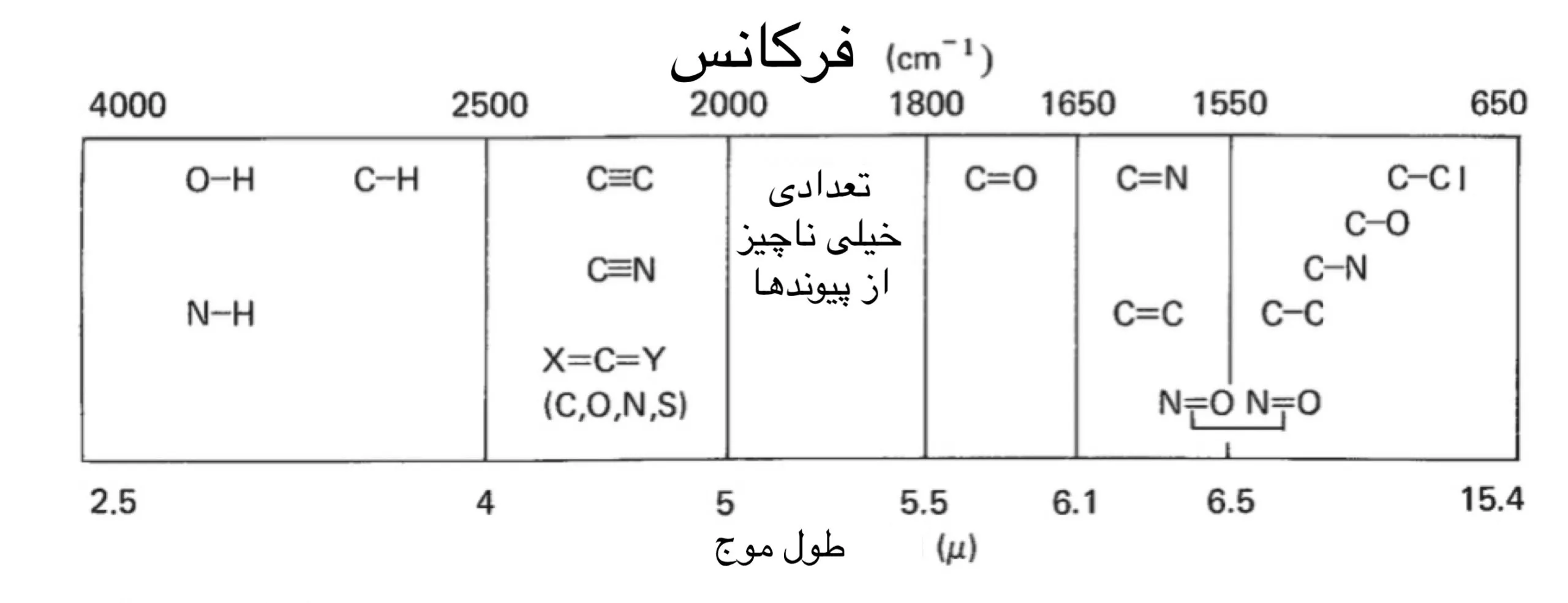
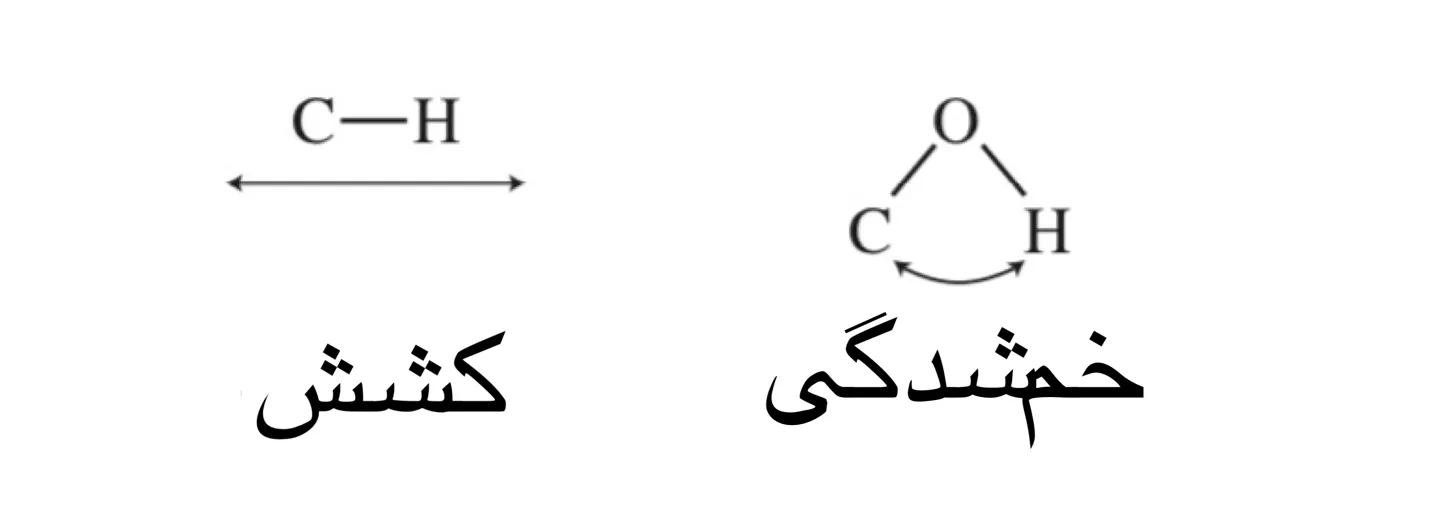
با این حال، انواع دیگر، پیچیده تر از کشش و خم شدن نیز هستند. تصاویر زیر برای حالات عادی ارتعاش یک گروه متیلن چندین اصطلاح را معرفی می کند. به طور کلی، ارتعاشات کششی نامتقارن در فرکانسهای بالاتر از ارتعاشات کششی متقارن همچنان رخ میدهد. همچنین، ارتعاشات کششی در فرکانس های بالاتر از ارتعاشات خمشی رخ می دهد. اصطلاحات برش خوردن، جنبیدن و چرخاندن معمولاً برای توصیف منشأ باندهای مادون قرمز استفاده می شود.
در هر گروهی از سه یا چند اتم که حداقل دو اتم آنها یکسان هستند، دو حالت کشش وجود دارد: متقارن و نامتقارن. نمونه هایی از این گروه بندی ها، در موارد زیر وجود دارد:
-CH3، -CH2-، -NO2، -NH2 و انیدریدها.
گروه متیل باعث ایجاد یک ارتعاش کششی متقارن در حدود 2872 سانتی متر-1 و یک کشش نامتقارن در حدود 2962 سانتی متر-1 می شود. گروه عاملی انیدرید به دلیل حالت کشش نامتقارن و متقارن دو پیوند در ناحیه C=O می دهد. یک پدیده مشابه در گروه آمینو نیز رخ می دهد، جایی که یک آمین اولیه (NH2) معمولاً دو ناحیه جذب کششی در N-H دارد، در حالی که یک آمین ثانویه (R2NH) فقط یک پیک جذب دارد. آمیدها نیز شرایط مشابهی دارند. دو قله کشش قوی N=O برای یک گروه نیترو وجود دارد که کشش متقارن در حدود 1350 سانتی متر-1 و کشش نامتقارن در حدود 1550 سانتی متر-1 ظاهر میشود.

این معادله برای محاسبه موقعیت تقریبی یک باند در طیف مادون قرمز با فرض اینکه K برای پیوندهای منفرد، دوگانه و سه گانه به ترتیب 5، 10، و 15 × 105 dynes/cm باشد، به کار میرود. در جدول 2.2 چند مثال آورده است. توجه داشته باشید که مقادیر این جدول، تطابقی عالی با مقادیر تجربی ارائه شده دارد. با این حال، مقادیر تجربی و محاسبه شده ممکن است به دلیل رزونانس، هیبریداسیون و سایر عوامل فعال و ایجاد اختلاف در مولکولهای آلی، با هم متفاوت باشند. با این وجود، مقادیر کیفی نسبتا مناسبی را میتوان با چنین محاسباتی به دست آورد.
دانلود ترجمه کتاب نگرشی بر طیف سنجی پاویا
2.5 طیف سنج مادون قرمز
ابزاری که طیف جذبی یک ترکیب را تعیین می کند، طیف سنج مادون قرمز یا به طور دقیقتر، اسپکتروفتومتر نامیده میشود. دو نوع طیفسنج مادون قرمز در آزمایشگاههای آلی بیشتر رایج هستند: ابزار پراکنده و ابزار تبدیل فوریه (FT). هر دوی این نوع ابزارها طیفی از ترکیبات را در محدوده مشترک 4000 تا 400 سانتی متر-1 ارائه می دهند. اگرچه این دو طیف تقریباً یکسانی را برای یک ترکیب خاص ارائه میکنند، طیفسنجهای مادون قرمز FT ، طیف مادون قرمز را بسیار سریعتر از ابزارهای پراکنده ، ارائه میکنند.
آ)طیفسنجهای پراکنده مادون قرمز
شکل 2.3 به طور شماتیک اجزای یک طیف سنج مادون قرمز پراکنده ساده را نشان می دهد. این ابزار پرتویی از تابش مادون قرمز را از یک سیم داغ تولید می کند و با استفاده از آینه، آن را به دو پرتو موازی با شدت برابر تقسیم میکند. نمونه در یک بخش قرار میگیرد و بخش دیگر به عنوان مرجع استفاده میشود. پرتوها سپس به تک رنگ میرسند، که هر کدام را در یک طیف پیوسته از فرکانسهای نور مادون قرمز پراکنده میکند. مونوکروماتور، از یک بخش به سرعت در حال چرخش (برش پرتو) تشکیل شده است که دو پرتو را به طور متناوب به یک توری پراش (یک منشور در ابزارهای قدیمی تر) منتقل می کند.
در طیفسنجی، نور یا امواج الکترومغناطیسی با انرژیهای مختلف به نمونه مورد نظر تابانده میشود. سپس تغییرات در این نور یا امواج پس از تعامل با نمونه، با استفاده از دستگاهها و تجهیزات مناسب اندازهگیری میشود. اطلاعات به دست آمده از این اندازهگیریها در قالب یک نمودار به نام “طیف” نمایش داده میشود که به محققان کمک میکند تا از ترکیبات موجود در نمونه و ویژگیهای آنها مطلع شوند.
توری پراش با چرخش آهسته، فرکانس یا طول موج تابش رسیدن به آشکارساز ترموکوپل را تغییر می دهد. آشکارساز نسبت بین شدت پرتوهای مرجع و نمونه را نشان میدهد. به این ترتیب، آشکارساز تعیین میکند که کدام فرکانس توسط نمونه جذب شده و کدام فرکانس تحت تأثیر نور عبوری از نمونه قرار نمیگیرد.

پس از تقویت سیگنال با آشکارساز، طیف حاصل از نمونه به وسیله ریکوردر بر روی نمودار ترسیم میشود. توجه به این نکته مهم است که طیف، با تغییر فرکانس تابش مادون قرمز و چرخش توری پراش، ثبت می شود. ابزارهای پراکنده طیفی جزو حوزه فرکانس است.
طیفسنجی به دلیل دقت و دقت بالای خود، در مطالعات مختلف بسیار مورد استفاده قرار میگیرد. برای مثال، در شیمی، این تکنیک به شناسایی و تحلیل ترکیبات شیمیایی کمک میکند و در فیزیک، امکان بررسی ویژگیهای الکترونی و فیزیکی مواد فراهم میآورد. همچنین، در زمینههایی مانند زیستشناسی و پزشکی، طیفسنجی به تشخیص بیماریها و بررسی ترکیبات موجود در انواع نمونهها کمک میکند.
با پیشرفت تکنولوژی، روشهای مختلفی برای انجام طیفسنجی توسعه یافته است که هر کدام ویژگیها و مزایای خاص خود را دارند. از جمله این روشها میتوان به طیفسنجی UV-Vis، طیفسنجی فروسرخ، طیفسنجی همجذبی نووسپین، و طیفسنجی رامان اشاره کرد که هر کدام در زمینهها و کاربردهای خاص خود مورد استفاده قرار میگیرند.
 مکاتب | فروشگاه دانلود کتاب
مکاتب | فروشگاه دانلود کتاب

نقد و بررسیها
هنوز بررسیای ثبت نشده است.